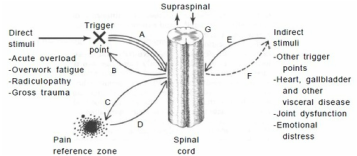
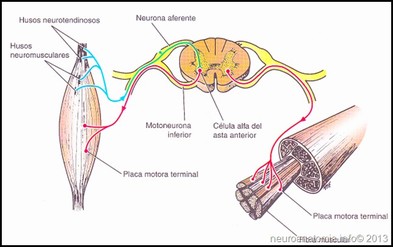
 INTRODUCCIÓN Los fisiólogos usan el término contractura específicamente para describir el acortamiento endógeno del aparato contráctil muscular en ausencia de actividad EMG iniciada por las células del asta anterior. Confusamente, el mismo término, la contractura, es utilizado por clínicos para describir la remodelación (acortamiento) del tejido conectivo que puede incluir cápsulas articulares, ligamentos y la reducción del número de sarcómeros. Estos cambios ocurren cuando el músculo permanece en una posición acortada durante un período prolongado de tiempo. Esta condición también carece de actividad de EMG, pero por una razón diferente. TENSIÓN MUSCULAR En cuanto a la variación de la tensión muscular, se ha establecido que depende de dos factores:
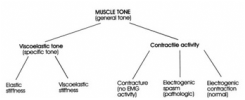 Clínicamente se utilizan dos términos para identificar la tensión muscular: tono muscular y espasmo muscular. Desafortunadamente, ambos términos son ambiguos porque se usan con significados conceptualmente diferentes. El tono muscular, como se aplica a la práctica clínica, es la resistencia al movimiento pasivo. Se pueden medir dos tipos de rigidez; elástica y viscoelástica. La hipertonía se utiliza generalmente para identificar un aumento del tono muscular por cualquier razón. Incluye una variedad de condiciones tales como espasticidad, rigidez, distonía y contractura muscular, que son entidades muy diferentes, El tono viscoelástico se distingue como una entidad separada y específica, al ser independiente de la actividad contráctil. Cualquier actividad contráctil se identifica a menudo como espasmo cuando ese término se utiliza en el sentido general. Sin embargo, la actividad contráctil puede ocurrir en tres formas diferentes:
 El significado específico del tono, se aplica sólo a cambios viscoelásticos en la ausencia de actividad muscular contráctil. Cualquier medida dinámica de rigidez muscular incluye el componente viscoelástico. La única forma de medir la rigidez elástica de un segmento corporal, es asegurar una ausencia de actividad contráctil electrogénica mediante una monitorización adecuada y no encontrar actividad EMG. Por lo tanto, la presencia o ausencia de actividad EMG es de fundamental importancia en cuanto a lo que se está midiendo. Algunos estudios observaron la sensibilidad de los cambios en la rigidez muscular antes y después de la anestesia y concluyeron que no había reducción del tono como resultado de la anestesia quirúrgica. Por lo tanto, el tono elástico del músculo en reposo normal debe ser causado por sus propiedades viscoelásticas en ausencia de actividad contráctil del músculo. En otros estudios donde se estudió el reflejo de espasmo local (REL), observaron la reproducción de dicho espasmo a través de la estimulación mecánica que desapareció tras la anestesia del nervio muscular que inervaba ese músculo o al cortarlo con unas tijeras.  FENÓMENO DE TIXOTROPÍA Una serie de materiales tales como pintura, el ketchup de tomate, y la sangre humana muestra la propiedad de la tixotropía. Cuando se agitan o vierten por primera vez, las sustancias tixotrópicas resisten la agitación o el movimiento. Después del movimiento inicial, su viscosidad disminuye, a menudo precipitadamente. La resistencia al movimiento depende fuertemente de la historia previa del movimiento. Un aumento del movimiento durante dos o tres ciclos puede causar una gran reducción en la resistencia al movimiento, reconocible a partir de la mayor amplitud del movimiento. Lakie y Robson (1988) exploraron con más detalle la tasa de recuperación de rigidez tixotrópica en reposo. Encontraron un aumento de ésta de tres veces después de 10 minutos, que continuó a una tasa decreciente que todavía podría ser detectada 24-30 horas más tarde. Las constantes de tiempo tixotrópicas pueden cubrir un rango considerable.  Una aplicación importante de la tixotropía es la práctica de los atletas que calienten antes del ejercicio precompetición. Esto libera la rigidez muscular tixotrópica acumulada. Por otra parte, la alta viscosidad de un músculo en reposo (por ejemplo, del erector espinal) puede ayudar a mantener una postura dada sin gasto de energía. La explicación más ampliamente aceptada para la tixotropía de los músculos es una tendencia para que los filamentos de actina y miosina se “peguen” cuando están inactivos durante un período de tiempo. 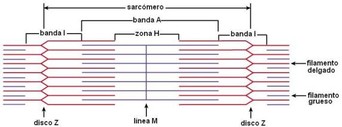 "Puede observarse una disminución tixotrópica marcada (hasta diez veces) en el músculo". La rigidez de un músculo cuando este se moviliza repentinamente, ayuda en gran medida a explicar como es capaz de mantenerse sin una actividad EMG mantenida en los músculos posturales. Se puede observar la presencia de algunas ráfagas de actividad EMG correctivas para mantener el equilibrio. El tono de reposo del músculo puede incluir un componente tixotrópico significativo. Aplicaciones clínicas El origen exacto del tono muscular no depende, por lo tanto, de la actividad motora. Aún más enigmático es el dolor de tejido blando relacionado con el movimiento que no está asociado con una rigidez aumentada y objetivamente demostrable. Se puede observar un aumento del tono específico en sujetos sanos. Además, podemos observar una disminución del mismo tono en sujetos sintomáticos. La relación entre tono muscular y el dolor, no es inherentemente un criterio clínico.  ESPASMO MUSCULAR La espasticidad es un término clínico comúnmente aplicado al músculo espasmódico observado en condiciones tales como hemiplejia o lesión de la médula espinal. Se asocia con hiperreflexia y/o con lesiones de las áreas premotoras o su salida a nivel medular. En pacientes con lesión de la médula espinal, el espasmo muscular es iniciado por cualquier entrada aferente en ese segmento de la columna vertebral, indicando una pérdida de la influencia inhibidora supraspinal en las neuronas motoras. Así, la espasticidad se puede pensar que ocurre en el nivel espinal debido a la pérdida de la inhibición supraspinal. La rigidez es claramente diferente de la espasticidad y de diferente etiología del sistema nervioso, aunque sus efectos también pueden ser causados por espasmo muscular. Es clinicamente caracterizado como "rigidez o inflexibilidad" que, por ejemplo, aparece temprano y progresa en la enfermedad de Parkinson. Dado que esta rigidez es causada por el desequilibrio entre las vías indirectas de los ganglios basales, se caracteriza por cocontracción de los músculos antagonistas, se puede considerar un espasmo muscular a nivel supraespinal. Un calambre muscular es comúnmente considerado como un espasmo muscular doloroso, como los calambres nocturnos en las piernas, podría servir como una definición clínica, sin embargo, la enfermedad de McArdle también se conoce como contractura dolorosa ( y libre de EMG).  Condiciones clínicas con aumento doloroso de la tensión muscular: Casi la mitad o más de los pacientes vistos por la mayoría los profesionales del dolor muscular no pueden ser diagnosticados de forma específica. CICLO ESPASMO-DOLOR-ESPASMO No se mantiene en pie ante la verificación experimental, ya sea desde el punto de vista fisiológico como clínico. Estudios fisiológicos muestran que el dolor muscular tiende a inhibir, no a facilitar, la actividad contráctil refleja de ese músculo. Comúnmente el músculo doloroso (aunque puede sentirse tenso) no muestra actividad EMG, es decir, no todos los músculos con espasmo (identificado con EMG) son dolorosos. Walsh explicó claramente como este concepto erróneo ha sido fuertemente reforzado por una mala interpretación de los reflejos motores humanos basándose en experimentos realizados en gatos, y como este error conceptual ha persistido a lo largo de todo el siglo XX. Otros autores resumieron la aplastante evidencia de que “el dolor muscular se encuentra estrechamente relacionado con el espasmo muscular” representa un mito que ha sido poderosamente fomentado por intereses comerciales. Desafortunadamente para esto teoría, generalmente no hay actividad de EMG y cuando hay, su momento e intensidad no se correlaciona con el dolor. El dolor parece ser una respuesta de desarrollo más lento al espasmo reflejo sostenido.  El término cefalea tensional representa un buen ejemplo de este mito en acción. El término se originó dando por hecho que el espasmo muscular era el responsable del dolor de cabeza y que la relajación de los músculos pericraneales lo aliviaría. En 1991, una publicación de la revista PAIN resaltó que era inequívocamente claro que la actividad EMG aumentada no podía explicar la hipersensibilidad a la presión sobre los músculos y el dolor de la cefalea tensional. Posteriormente salió a la luz un término “modernizado” del concepto, denominado estrés-hiperactividad-dolor, parece también invalidada por los mismos motivos.  Movimiento y actividad EMG La limitación del rango de movimiento de un músculo se estima clínicamente extendiendo lentamente el músculo hasta que alcanza una barrera de tensión creciente. Esta barrera tiene el efecto de acortar el músculo. Esta prueba por sí sola no distingue entre el aumento de la tensión viscoelástica, la espasticidad, la contractura fisiológica y la fibrosis. Cuando esta prueba muestra mayor rango de movimiento (hipermovilidad) a veces se interpreta como disminución del tono muscular. Sin embargo, esta interpretación de esta prueba por sí sola no es fiable porque la hipermovilidad puede ser provocada por la laxitud de los elementos del tejido conectivo ligamentoso y capsular o por una disfunción de la actividad contráctil muscular.  En un estudio sobre movimiento lumbar y la actividad EMG, se observó que éstas variables estaban altamente relacionadas cuando los sujetos fueron sin dolor, pero no cuando tenían dolor. Estos autores también observaron un retraso entre la actividad muscular y el dolor, con aumento de la tensión muscular que precede al dolor. Esta falta de correlación entre el dolor muscular y el aumento de la actividad EMG se aplica también a la literatura sobre el dolor lumbar. Cuando la actividad EMG es involuntaria (espasmo) y está presente en pacientes que se quejan de dolor, no se puede suponer que el espasmo esté causando el dolor. El espasmo per se puede causar dolor, y en ese caso, la cantidad de espasmo y el dolor se correlacionará de forma cercana; pero algo más que el dolor muscular está causando el espasmo. En otro estudio, un grupo de nueve pacientes que se quejaron de dolor lumbar y que tenían un “espasmo” palpable paraspinal, mostraron cierta actividad EMG casi continuamente durante la noche. Se suponía que un “ciclo vicioso espasmódico“ relacionaba los dos variables. Cinco de los pacientes fueron diagnosticados como dolor miofascial debido a puntos gatillo (PG). Cada vez hay más pruebas de que los PG pueden inducir espasmo muscular en otros músculos que los que albergan el PG. Los otros 4 sujetos no han podido ser clasificados en un diagnostico en particular ( dolor lumbar inespecífico). El tejido ligamentario, la disfunción articular y los PG pueden inducir espasmo muscular en los músculos asociados. Estas tres condiciones pueden ser dolorosas en presencia o ausencia de espasmo muscular. 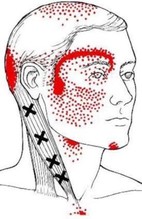 INTRODUCCIÓN DEL SINDROME DE DOLOR MIOFASCIAL Durante muchos años se ha postulado que el dolor muscular era un problema secundario a otros diagnósticos, aunque la evidencia más actual es abrumadora y acredita que el dolor muscular puede ser una causa de disfunción primaria. Éste cambio de paradigma ha surgido en base a los estudios en el campo del dolor crónico, ya que éste se ha establecido como una entidad de enfermedad por si misma y no la causa sintomática de cualquier otra patología. Los PG pueden provocar a nivel somático, disfunciones motoras, por ejemplo, debilidad muscular, inhibición, incremento de la irritabilidad motora, espasmo, desequilibrio muscular y alteraciones en el reclutamiento motor, tanto en el músculo afectado como en músculos funcionalmente relacionados. A nivel clínico podemos diferenciar los PG activos y latentes, que dan lugar a hallazgos similares en la exploración física. La diferencia es que los PG latentes no reproducen ningún síntoma de manera espontánea. Cabe destacar que los PG latentes pueden ser fácilmente convertidos en activos, al menos en parte, debido al grado de sensibilización y del incremento de la eficacia sináptica en el asta dorsal de la médula. 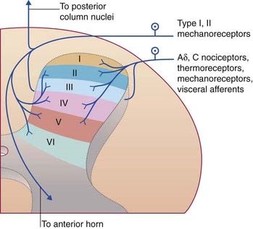 El grado de sensibilización y la eficacia sináptica del asta dorsal pueden inducir un aumento de la percepción del dolor debido a la liberación de sustancias algogénicas en las láminas de Rexed del asta posterior de la médula, con el consiguiente aumento de la hiperalgesia periférica local y referida. Existen diferentes teorías y modelos neurofisiológicos para explicar la reproducción del dolor referido debido a la presencia de PG: - Teoría de la proyección convergente. - Teoría de la facilitación de la convergencia. - Teoría del reflejo axonal. - Teoría de la convergencia talámica. - Teoría de la hiperexcitabilidad central. 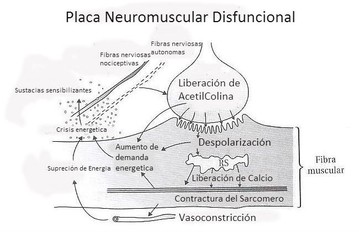 ASPECTOS NEUROFISIOLÓGICOS DE LOS PG MUSCULARES Es importante dejar claro, como venimos diciendo reiteradamente, que las contracturas no son lo mismo que las espasmos musculares. Las contracturas no requieren de actividad EMG y se postula que su origen endógeno no afecta a todo el músculo. Además, se puede sugerir que no tienen un tratamiento particularmente eficaz. Los espasmos musculares implican actividad electrogénica e implican que la actividad de la motoneurona alfa y la placa neuromuscular estén activas. Dolor muscular Los impulsos nociceptivos son transmitidos a través de neuronas de segundo orden localizadas en el asta dorsal y viajan en la médula espinal hasta áreas somatosensoriales primarias y secundarias del cerebro, tal como la amígdala, la circunvolución cingulada central y la corteza sensitiva primaria. Cuando los neuropéptidos son liberados en cantidades suficientes dan lugar a la liberación de histamina, bradicinina, etc. El dolor referido se origina en el asta dorsal y es el resultado de la activación de conexiones axonales entre fibras nerviosas nociceptivas de las neuronas del asta dorsal, las cuales en situación de normalidad se mantienen silentes y son activadas por los mecanismos de la sensibilización central. . Las contracturas múltiples que se observan en los músculos de los pacientes con dolor miofascial posiblemente dan lugar a la compresión de los capilares regionales, con isquemia e hipoxia. La hipoxia puede desencadenar un incremento inmediato de la liberación de AcetilColina (AC) en la placa motora. La hipoxia también induce una disminución del pH local con activación de los receptores del potencial receptor transitorio vaniloide (TRPV) y de los canales iónicos sensibles al ácido (ASIC) por medio de iones de hidrógeno o de protones. Dado que estos canales son nociceptivos, inician respuestas de dolor, hiperalgesia y sensibilización central sin inflamación y sin otros signos de lesión o traumatismo en el músculo. Es probable que en los aspectos sensitivos de los PG haya tipos múltiples de ASIC implicados, tal como el ASIC1a (que procesa los estímulos lesivos) y el ASIC3 (que está implicado en el dolor asociado a la inflamación). El pH bajo reduce la cantidad de AC esterasa en la unión neuromuscular y puede desencadenar la liberación de varios neurotransmisores y de mediadores inflamatorios, tal como el CGRP, la sustancia P, bradicinina, las interleucinas, el ATP, la serotonina, las prostaglandinas, el potasio y los protones, todo lo cual daría lugar a una disminución en el umbral mecánico y en la activación de los receptores nociceptivos periféricos. FISIOPATOLOGÍA DE LOS PG: LA HIPÓTESIS INTEGRADA La hipótesis de que cada PG contiene un sitio sensitivo, es decir, un sitio en el que se puede inducir un reflejo de espasmo local (REL) cuando se estimula mecánicamente el PG, y un sitio activo motor considerado como una zona a partir de la cual se registra una actividad eléctrica espontánea (SEA). En este modelo, el sitio sensitivo contiene nociceptores y representa el componente sensitivo, mientras que el sitio activo está constituido por placas motoras disfuncionales que podrían corresponder al componente motor. La lesión del retículo sarcoplásmico o de la membrana celular da lugar a un incremento de la concentración de calcio, un acortamiento de los filamentos de actina y miosina, una escasez de ATP y una alteración de la bomba del calcio. Simons y Travell propusieron la denominada «hipótesis de la crisis energética». La hipótesis de la crisis energética se ha transformado en la denominada hipótesis integrada de los puntos gatillo. La hipótesis integrada es el concepto teórico más aceptado. La hipótesis integrada propone la posibilidad de que la despolarización anómala de la membrana postsináptica de la placa motora dé lugar a una crisis energética hipóxica localizada que está asociada a arcos reflejos sensitivos y autonómicos mantenidos por mecanismos de sensibilización complejos.  Se observó la presencia de actividad EMG espontánea en un PG de la parte superior del músculo trapecio. Los autores de este estudio describieron dos componentes de esta actividad EMG espontánea: una actividad de fondo constante y de amplitud baja con 50 mV, y una actividad intermitente de amplitud alta y con picos de 100-700 mV. Otros investigadores confirmaron la actividad de fondo constante de 10-50 mV y ocasionalmente de 80 mV en el PG. El origen de esta SEA es todavía controvertido; sin embargo, hay evidencia concluyente en apoyo de que la SEA se origine a partir de potenciales de placa motora (EPP). Simons llegó a la conclusión de que la SEA es igual que el ruido de la placa motora (EPN). El EPN muestra una prevalencia mayor en los PG activos que en los PG latentes. El EPN parece reflejar una despolarización local de las fibras musculares inducida por un incremento significativo y anómalo de la liberación espontánea de AC. En un modelo animal, demostraron que es posible reducir la SEA mediante la toxina botulínica, que inhibe la liberación de AC en la unión neuromuscular. Por otra parte, en el análisis de los comportamientos motores de un PG se ha observado que la actividad EMG intramuscular en los PG presenta comportamientos motores similares a los de la actividad EMG de superficie sobre un PG, un resultado que apoya la posibilidad de que la actividad eléctrica proceda de las placas motoras extrafusales y no de las intrafusales (husos musculares). Desde una perspectiva clínica, en varios estudios se ha observado que el tratamiento de los PG puede eliminar o reducir significativamente el EPN. Los resultados obtenidos en estos estudios apoyan la posibilidad de que los PG estén relacionados con placas motoras disfuncionales. En lo que se refiere al componente motor de los PG, la actividad EMG intramuscular y de superficie registrada a partir de un PG demostró que la SEA es similar a un potencial de espasmo muscular y, en segundo lugar, que el incremento de la intensidad del dolor muscular local se correlaciona positivamente con la duración y la amplitud de los espasmos musculares. Los espasmos musculares localizados pueden inducir hipoxia intramuscular, aumento de las concentraciones de los mediadores algogénicos, estimulación mecánica directa de los nociceptores y dolor. Por tanto, parece que el dolor y la sensibilidad dolorosa a la palpación asociados a los PG están estrechamente relacionados con la isquemia focal sostenida y con los espasmos musculares en el interior de las bandas tensas musculares. FACILITACIÓN SIMPÁTICA DEL DOLOR LOCAL Y DOLOR REFERIDO MUSCULAR
Hay un interés creciente por la asociación entre los PG y el sistema nervioso simpático. En estudios efectuados sobre seres humanos se ha demostrado que el incremento de la descarga eferente simpática aumenta la frecuencia y la amplitud de la actividad EMG de los PG musculares, al tiempo que los bloqueadores simpáticos disminuyen la frecuencia y la amplitud de la actividad EMG. Otros investigadores han señalado que los bloqueadores simpáticos disminuyen la sensibilidad al dolor relacionado con los PG y con los puntos dolorosos, un resultado que es congruente con la observación del aumento de las concentraciones de norepinefrina en los PG activos. Otros autores en el año 2006, señalaron que la facilitación simpática inducía una disminución en los umbrales del dolor a la presión y en el umbral de presión para la aparición de dolor referido, así como un incremento en la intensidad del dolor local y del dolor referido, lo que sugiere una interacción simpático-sensitiva en los PG. En el año 2009, detectaron una disminución de la respuesta del flujo sanguíneo cutáneo tras la estimulación dolorosa de PG latentes, en comparación con la estimulación de zonas distintas de los PG, un resultado que se podría explicar por el incremento de la actividad de vasoconstricción simpática en los PG latentes. La sensibilidad PG parece ser dependiente de la hiperactividad simpática. El aumento de la actividad simpática en los PG puede incrementar la liberación de norepinefrina y de ATP, entre otros compuestos. Otro posible mecanismo sería que el aumento del nivel de la actividad nerviosa simpática muscular diera lugar a un retraso en la resolución de las sustancias inflamatorias y de los cambios en el entorno químico local de los PG. Tal como se ha señalado previamente, se propuso la posibilidad de que la presencia de receptores adrenérgicos a y b en la placa motora pudiera representar un mecanismo de la interacción, aunque dicha posibilidad no ha sido confirmada en el ser humano.
0 Comentarios
|
AutorGurdiel F. Archivos
Diciembre 2017
|